ترسيب (كيمياء) من ويكيبيديا، الموسوعة الحرة
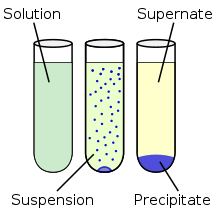
الترسيب الكيميائي
الترسيب في الكيمياء هو عملية تشكل جسم صلب في محلول من خلال تفاعل كيميائي. عندما يحدث التفاعل في محلول سائل فإن المادة الصلبة المتشكلة تعرف باسم الراسب، ويدعى التفاعل الذي يؤدي إلى حدوث تشكل الراسب باسم تفاعل ترسيب. هناك أنواع محددة من الرواسب التي لا ترقد (عملية رسوب) إلى أسفل إناء التفاعل نتيجة الجاذبية، بل تبقى على شكل مستعلق في المحلول، والتي يمكن تحويله إلى راسب بإجراء عملية تثفيل.
يمكن أن تتم عملية ترسيب الأجسام الصلبة وفق متطلبات محددة من أجل تحضير الجسيمات النانوية.
تستخدم تفاعلات الترسيب من أجل صنع الخضب ومن أجل إزالة الأملاح من الماء أثناء معالجة المياه، وكذلك في التحليل النوعي في الكيمياء اللاعضوية. كما تستخدم تفاعلات الترسيب أيضاً في الكيمياء العضوية من أجل عزل المركبات المرجوة أثناء تفاعلات الاصطناع العضوي، حيث يحصل على المادة على شكل بلورات.
أمثلة

من الأمثلة على تفاعلات الترسيب العضوية التفاعل بين البورفيرين في تقطير مرتد مع حمض البروبيونيك، ثم بتبريد مزيج التفاعل إلى درجة حرارة الغرفة، ثم بإجراء عملية ترشيح.
المراجع
عمليات كيميائية
عمليات الفصل

الترسيب الكيميائي
الترسيب في الكيمياء هو عملية تشكل جسم صلب في محلول من خلال تفاعل كيميائي. عندما يحدث التفاعل في محلول سائل فإن المادة الصلبة المتشكلة تعرف باسم الراسب، ويدعى التفاعل الذي يؤدي إلى حدوث تشكل الراسب باسم تفاعل ترسيب. هناك أنواع محددة من الرواسب التي لا ترقد (عملية رسوب) إلى أسفل إناء التفاعل نتيجة الجاذبية، بل تبقى على شكل مستعلق في المحلول، والتي يمكن تحويله إلى راسب بإجراء عملية تثفيل.
يمكن أن تتم عملية ترسيب الأجسام الصلبة وفق متطلبات محددة من أجل تحضير الجسيمات النانوية.
تستخدم تفاعلات الترسيب من أجل صنع الخضب ومن أجل إزالة الأملاح من الماء أثناء معالجة المياه، وكذلك في التحليل النوعي في الكيمياء اللاعضوية. كما تستخدم تفاعلات الترسيب أيضاً في الكيمياء العضوية من أجل عزل المركبات المرجوة أثناء تفاعلات الاصطناع العضوي، حيث يحصل على المادة على شكل بلورات.
أمثلة
من الأمثلة على تفاعلات الترسيب اللاعضوية التفاعل بين نترات الفضة مع محلول من كلوريد الصوديوم، حيث يترسب كلوريد الفضة على شكل راسب أبيض، كما في التفاعل التالي: N a C l ( a q ) + A g N O 3 ( a q ) ⟶ N a + + N O 3 − + A g C l ( s ) ↓ {\displaystyle \mathrm {NaCl_{\ (aq)}+AgNO_{3\ (aq)}\longrightarrow Na^{+}+NO_{3}^{-}+AgCl_{\ (s)}\downarrow } }
من الأمثلة على تفاعلات الترسيب العضوية التفاعل بين البورفيرين في تقطير مرتد مع حمض البروبيونيك، ثم بتبريد مزيج التفاعل إلى درجة حرارة الغرفة، ثم بإجراء عملية ترشيح.
المراجع
Dhara, S. (2007). "Formation, Dynamics, and Characterization of Nanostructures by Ion Beam Irradiation". Critical Reviews in Solid State and Materials Sciences. 32 (1): 1–50. :10.1080/10408430601187624
A. D. Adler; F. R. Longo; J. D. Finarelli; J. Goldmacher; J. Assour; L. Korsakoff (1967). "A simplified synthesis for meso-tetraphenylporphine". J. Org. Chem. 32 (2): 476–476.
10.1021/jo01288a053
10.1021/jo01288a053
تشكيل، الديناميات، وتوصيف النانوية التي كتبها ايون شعاع
نبذة مختصرة
أيون شعاع الإشعاع هو أداة محتملة لتشكيل المرحلة وتعديل المواد كأسلوب عدم التوازن. ارتفاع محلية في درجة الحرارة وفائقة السرعة (~10 -12 ق) الإنقشاع من المساس الطاقة وجعله أداة جاذبة للتشكيل مرحلة متبدل الاستقرار. كما واقع الأمر، ويهيمن عنصرا رئيسيا في علوم المواد عن طريق وسائل شعاع أيون، إما لتخليق المواد أو لتوصيف لها. وسوف تناقش تركيب النانو، وتعديلها بواسطة تقنية شعاع ايون في هذه المقالة الاستعراض. وسيتم مناقشة تشكيل النانو باستخدام تقنية شعاع أيون أولا. اعتمادا على الأنواع (على سبيل المثال، كتلة وولاية تهمة) ومجموعة الطاقة، وهناك طرق مختلفة لايون حيوية لتبديد الطاقة. كما سيتم تغطية دور الإلكترون في هذه المقالة كمبدأ أساسي من تفاعله مع المادة، التي هي نفسها بالنسبة للأيون. باستخدام
شعاع أيون رد الفعل البسيط أو الإلكترون الناجم عن ترسب، يمكن الأنوية
مرحلة الثانوية من خلال تقنيات خلط شعاع أيون، إما عن طريق استخدام التشعيع
غاز خامل أو رد الفعل زرع الغاز على أي ركيزة المطلوب. التنوي من المرحلة الثانوية ويمكن أيضا أن يتم تنفيذها بواسطة أشعة الإلكترون وغرس المباشر إما أيونات سلبية أو إيجابية. مطلوبة عمليات الصلب زرع في مرحلة ما بعد للنمو الكامل للمجموعات شكلت في معظم تقنيات أيون إشعاع هذه. عمليات زرع أن يكون متلازما تقنية عدم التوازن والعيوب دائما دورا تلعبه في تشكيل المرحلة، amorphization، وخارجها (تشكيل نفطة). عندما زرعت مع طاقة كبيرة، حتى الإلكترونات، واحدة من الجزيئات الأخف وزنا مشحونة، كما تظهر هذه الخصائص. خسائر الطاقة الإلكترونية والنووية من الجسيمات المشحونة التي تؤثر تلعب دورا حاسما في تعديل جوهري. المنشطات لnanocluster، ومع ذلك، لا يزال موضوعا مثيرا للجدل. سيتم إلقاء بعض الضوء على هذا الموضوع بمناقشة شعاع الأيون.
عمليات الفصل

ليست هناك تعليقات:
إرسال تعليق